Recent glacial retreat and its impact on hydrological processes on the Tibetan Plateau, China, and surrounding regions
1
2007
... 青藏高原地区是中低纬度山地冰川发育最广泛的地区,近年来,随着全球气候持续变暖,青藏高原地区的冰川正经历着快速的消融退缩[1].冰尘是冰川消融区表面暗色物质的重要组成部分,是由有机物质、无机矿物颗粒和微生物群落相互结合形成的黑色或棕色的球状聚合体[2].冰尘广泛存在于冰川消融区表面,其存在形式主要有两种,一种是冰尘穴,是冰川表面充满冰川融水和生物活性沉积物的圆柱体洞穴;另一种是冰尘颗粒,在喜马拉雅冰川和中国西部的山地冰川表面,冰尘主要以冰尘颗粒的形式存在[3].冰尘颗粒的生长具有明显的季节性,并且具有生长、裂解交替循环的生命周期[4-5].在冰川消融期(5—10月),冰川表面融水丰富,温度日照适宜,在微生物的作用下,消融区表面会形成表面被丝状蓝藻包裹,内部均匀分布无机颗粒和有机物质的冰尘颗粒[4,6];到冬季(11月—次年4月)由于冰川表面没有融水支持,部分冰尘颗粒会进入休眠阶段而停止生长,另一部分冰尘颗粒则会发生裂解,裂解形成的碎片在生长期重新发育成新的冰尘[4]. ...
A large amount of biogenic surface dust (cryoconite) on a glacier in the Qilian Mountains, China
1
2005
... 青藏高原地区是中低纬度山地冰川发育最广泛的地区,近年来,随着全球气候持续变暖,青藏高原地区的冰川正经历着快速的消融退缩[1].冰尘是冰川消融区表面暗色物质的重要组成部分,是由有机物质、无机矿物颗粒和微生物群落相互结合形成的黑色或棕色的球状聚合体[2].冰尘广泛存在于冰川消融区表面,其存在形式主要有两种,一种是冰尘穴,是冰川表面充满冰川融水和生物活性沉积物的圆柱体洞穴;另一种是冰尘颗粒,在喜马拉雅冰川和中国西部的山地冰川表面,冰尘主要以冰尘颗粒的形式存在[3].冰尘颗粒的生长具有明显的季节性,并且具有生长、裂解交替循环的生命周期[4-5].在冰川消融期(5—10月),冰川表面融水丰富,温度日照适宜,在微生物的作用下,消融区表面会形成表面被丝状蓝藻包裹,内部均匀分布无机颗粒和有机物质的冰尘颗粒[4,6];到冬季(11月—次年4月)由于冰川表面没有融水支持,部分冰尘颗粒会进入休眠阶段而停止生长,另一部分冰尘颗粒则会发生裂解,裂解形成的碎片在生长期重新发育成新的冰尘[4]. ...
Characteristics of surface dust on Urumqi Glacier No. 1 in the Tien Shan mountains, China
1
2008
... 青藏高原地区是中低纬度山地冰川发育最广泛的地区,近年来,随着全球气候持续变暖,青藏高原地区的冰川正经历着快速的消融退缩[1].冰尘是冰川消融区表面暗色物质的重要组成部分,是由有机物质、无机矿物颗粒和微生物群落相互结合形成的黑色或棕色的球状聚合体[2].冰尘广泛存在于冰川消融区表面,其存在形式主要有两种,一种是冰尘穴,是冰川表面充满冰川融水和生物活性沉积物的圆柱体洞穴;另一种是冰尘颗粒,在喜马拉雅冰川和中国西部的山地冰川表面,冰尘主要以冰尘颗粒的形式存在[3].冰尘颗粒的生长具有明显的季节性,并且具有生长、裂解交替循环的生命周期[4-5].在冰川消融期(5—10月),冰川表面融水丰富,温度日照适宜,在微生物的作用下,消融区表面会形成表面被丝状蓝藻包裹,内部均匀分布无机颗粒和有机物质的冰尘颗粒[4,6];到冬季(11月—次年4月)由于冰川表面没有融水支持,部分冰尘颗粒会进入休眠阶段而停止生长,另一部分冰尘颗粒则会发生裂解,裂解形成的碎片在生长期重新发育成新的冰尘[4]. ...
天山哈密榆树沟冰川冰尘特征及其成因
3
2014
... 青藏高原地区是中低纬度山地冰川发育最广泛的地区,近年来,随着全球气候持续变暖,青藏高原地区的冰川正经历着快速的消融退缩[1].冰尘是冰川消融区表面暗色物质的重要组成部分,是由有机物质、无机矿物颗粒和微生物群落相互结合形成的黑色或棕色的球状聚合体[2].冰尘广泛存在于冰川消融区表面,其存在形式主要有两种,一种是冰尘穴,是冰川表面充满冰川融水和生物活性沉积物的圆柱体洞穴;另一种是冰尘颗粒,在喜马拉雅冰川和中国西部的山地冰川表面,冰尘主要以冰尘颗粒的形式存在[3].冰尘颗粒的生长具有明显的季节性,并且具有生长、裂解交替循环的生命周期[4-5].在冰川消融期(5—10月),冰川表面融水丰富,温度日照适宜,在微生物的作用下,消融区表面会形成表面被丝状蓝藻包裹,内部均匀分布无机颗粒和有机物质的冰尘颗粒[4,6];到冬季(11月—次年4月)由于冰川表面没有融水支持,部分冰尘颗粒会进入休眠阶段而停止生长,另一部分冰尘颗粒则会发生裂解,裂解形成的碎片在生长期重新发育成新的冰尘[4]. ...
... [4,6];到冬季(11月—次年4月)由于冰川表面没有融水支持,部分冰尘颗粒会进入休眠阶段而停止生长,另一部分冰尘颗粒则会发生裂解,裂解形成的碎片在生长期重新发育成新的冰尘[4]. ...
... [4]. ...
天山哈密榆树沟冰川冰尘特征及其成因
3
2014
... 青藏高原地区是中低纬度山地冰川发育最广泛的地区,近年来,随着全球气候持续变暖,青藏高原地区的冰川正经历着快速的消融退缩[1].冰尘是冰川消融区表面暗色物质的重要组成部分,是由有机物质、无机矿物颗粒和微生物群落相互结合形成的黑色或棕色的球状聚合体[2].冰尘广泛存在于冰川消融区表面,其存在形式主要有两种,一种是冰尘穴,是冰川表面充满冰川融水和生物活性沉积物的圆柱体洞穴;另一种是冰尘颗粒,在喜马拉雅冰川和中国西部的山地冰川表面,冰尘主要以冰尘颗粒的形式存在[3].冰尘颗粒的生长具有明显的季节性,并且具有生长、裂解交替循环的生命周期[4-5].在冰川消融期(5—10月),冰川表面融水丰富,温度日照适宜,在微生物的作用下,消融区表面会形成表面被丝状蓝藻包裹,内部均匀分布无机颗粒和有机物质的冰尘颗粒[4,6];到冬季(11月—次年4月)由于冰川表面没有融水支持,部分冰尘颗粒会进入休眠阶段而停止生长,另一部分冰尘颗粒则会发生裂解,裂解形成的碎片在生长期重新发育成新的冰尘[4]. ...
... [4,6];到冬季(11月—次年4月)由于冰川表面没有融水支持,部分冰尘颗粒会进入休眠阶段而停止生长,另一部分冰尘颗粒则会发生裂解,裂解形成的碎片在生长期重新发育成新的冰尘[4]. ...
... [4]. ...
Characteristics of cryoconite holes on a Himalayan glacier, Yala Glacier Central Nepal
1
2000
... 青藏高原地区是中低纬度山地冰川发育最广泛的地区,近年来,随着全球气候持续变暖,青藏高原地区的冰川正经历着快速的消融退缩[1].冰尘是冰川消融区表面暗色物质的重要组成部分,是由有机物质、无机矿物颗粒和微生物群落相互结合形成的黑色或棕色的球状聚合体[2].冰尘广泛存在于冰川消融区表面,其存在形式主要有两种,一种是冰尘穴,是冰川表面充满冰川融水和生物活性沉积物的圆柱体洞穴;另一种是冰尘颗粒,在喜马拉雅冰川和中国西部的山地冰川表面,冰尘主要以冰尘颗粒的形式存在[3].冰尘颗粒的生长具有明显的季节性,并且具有生长、裂解交替循环的生命周期[4-5].在冰川消融期(5—10月),冰川表面融水丰富,温度日照适宜,在微生物的作用下,消融区表面会形成表面被丝状蓝藻包裹,内部均匀分布无机颗粒和有机物质的冰尘颗粒[4,6];到冬季(11月—次年4月)由于冰川表面没有融水支持,部分冰尘颗粒会进入休眠阶段而停止生长,另一部分冰尘颗粒则会发生裂解,裂解形成的碎片在生长期重新发育成新的冰尘[4]. ...
Structure and formation process of cryoconite granules on Urumqi Glacier No. 1, Tien Shan, China
1
2010
... 青藏高原地区是中低纬度山地冰川发育最广泛的地区,近年来,随着全球气候持续变暖,青藏高原地区的冰川正经历着快速的消融退缩[1].冰尘是冰川消融区表面暗色物质的重要组成部分,是由有机物质、无机矿物颗粒和微生物群落相互结合形成的黑色或棕色的球状聚合体[2].冰尘广泛存在于冰川消融区表面,其存在形式主要有两种,一种是冰尘穴,是冰川表面充满冰川融水和生物活性沉积物的圆柱体洞穴;另一种是冰尘颗粒,在喜马拉雅冰川和中国西部的山地冰川表面,冰尘主要以冰尘颗粒的形式存在[3].冰尘颗粒的生长具有明显的季节性,并且具有生长、裂解交替循环的生命周期[4-5].在冰川消融期(5—10月),冰川表面融水丰富,温度日照适宜,在微生物的作用下,消融区表面会形成表面被丝状蓝藻包裹,内部均匀分布无机颗粒和有机物质的冰尘颗粒[4,6];到冬季(11月—次年4月)由于冰川表面没有融水支持,部分冰尘颗粒会进入休眠阶段而停止生长,另一部分冰尘颗粒则会发生裂解,裂解形成的碎片在生长期重新发育成新的冰尘[4]. ...
Bipolar dispersal of red-snow algae
1
2018
... 冰川表面的微生物群落通过与环境的相互作用,对冰川反照率和冰川融化速率存在显著影响[7-8].冰尘是冰川表面微生物重要的栖息地[9-11],冰尘中的微生物群落主要包括藻类、古细菌、细菌、真菌、原生生物和病毒[11],细菌群落以蓝藻、绿塑菌、变形菌门、拟杆菌门和放线菌门为主[12].冰尘中的微生物在利用溶解性有机质(DOM)的同时会不断产生新的DOM[13].冰川表面DOM通过冰川融水被重新分配到其他环境,为营养匮乏的冰川环境提供营养和能量来源[14].因此,冰尘在冰川物质能量平衡、冰川生物地球化学循环特别是碳循环中发挥着重要作用.有研究表明,在极地冰川表面DOM循环过程中,光化学过程和生物过程之间存在着相互作用的关系[15].一方面,光降解可导致DOM完全氧化为CO2或部分氧化形成新的DOM,导致DOM化学组成发生改变[16-18];另一方面,冰川表面强烈的紫外辐射会伤害微生物细胞,改变微生物的活动和群落组成[19],从而显著改变DOM的化学组成[20].因此,分析山地冰川表面冰尘中DOM的“光-生物”演化过程对研究消融期山地冰川表面DOM的演化过程至关重要. ...
Physically based model of the contribution of red snow algal cells to temporal changes in albedo in northwest Greenland
1
2020
... 冰川表面的微生物群落通过与环境的相互作用,对冰川反照率和冰川融化速率存在显著影响[7-8].冰尘是冰川表面微生物重要的栖息地[9-11],冰尘中的微生物群落主要包括藻类、古细菌、细菌、真菌、原生生物和病毒[11],细菌群落以蓝藻、绿塑菌、变形菌门、拟杆菌门和放线菌门为主[12].冰尘中的微生物在利用溶解性有机质(DOM)的同时会不断产生新的DOM[13].冰川表面DOM通过冰川融水被重新分配到其他环境,为营养匮乏的冰川环境提供营养和能量来源[14].因此,冰尘在冰川物质能量平衡、冰川生物地球化学循环特别是碳循环中发挥着重要作用.有研究表明,在极地冰川表面DOM循环过程中,光化学过程和生物过程之间存在着相互作用的关系[15].一方面,光降解可导致DOM完全氧化为CO2或部分氧化形成新的DOM,导致DOM化学组成发生改变[16-18];另一方面,冰川表面强烈的紫外辐射会伤害微生物细胞,改变微生物的活动和群落组成[19],从而显著改变DOM的化学组成[20].因此,分析山地冰川表面冰尘中DOM的“光-生物”演化过程对研究消融期山地冰川表面DOM的演化过程至关重要. ...
The cryoconite ecosystem on the Greenland ice sheet
2
2010
... 冰川表面的微生物群落通过与环境的相互作用,对冰川反照率和冰川融化速率存在显著影响[7-8].冰尘是冰川表面微生物重要的栖息地[9-11],冰尘中的微生物群落主要包括藻类、古细菌、细菌、真菌、原生生物和病毒[11],细菌群落以蓝藻、绿塑菌、变形菌门、拟杆菌门和放线菌门为主[12].冰尘中的微生物在利用溶解性有机质(DOM)的同时会不断产生新的DOM[13].冰川表面DOM通过冰川融水被重新分配到其他环境,为营养匮乏的冰川环境提供营养和能量来源[14].因此,冰尘在冰川物质能量平衡、冰川生物地球化学循环特别是碳循环中发挥着重要作用.有研究表明,在极地冰川表面DOM循环过程中,光化学过程和生物过程之间存在着相互作用的关系[15].一方面,光降解可导致DOM完全氧化为CO2或部分氧化形成新的DOM,导致DOM化学组成发生改变[16-18];另一方面,冰川表面强烈的紫外辐射会伤害微生物细胞,改变微生物的活动和群落组成[19],从而显著改变DOM的化学组成[20].因此,分析山地冰川表面冰尘中DOM的“光-生物”演化过程对研究消融期山地冰川表面DOM的演化过程至关重要. ...
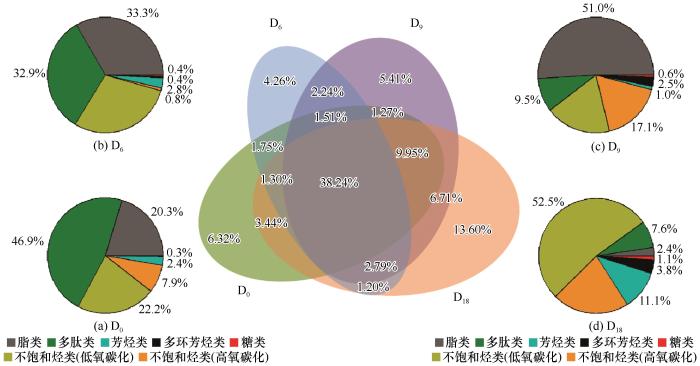
... 有研究表明,冰尘是冰川表面微生物重要的聚集区[9-11],冰尘中微生物群落非常丰富[11].结合老虎沟12号冰川新鲜冰尘中DOM脂类(25.88%)和多肽类(20.11%)的含量,以及新鲜冰尘DOM的光谱斜率的比值SR=1.93(SR>1),说明新鲜冰尘中DOM主要源自冰尘内部的微生物活动[41,54].同时,老虎沟12号冰川地处干旱和半干旱环绕区,西边是塔里木盆地的塔克拉玛干沙漠,西南与柴达木盆地毗邻,北部是大面积的戈壁沙漠[55],因此,陆源性输入也是冰尘中DOM的重要来源,主要体现在新鲜冰尘中含有大量的低氧碳比的不饱和烃类(31.83%)和高氧碳比的不饱和烃类(18.12%),包括木质素以及单宁类化合物[56]通过风媒或干湿沉降传输到冰川表面. ...
Microbial community variation in cryoconite granules on Qaanaaq Glacier, NW Greenland
0
2016
The microorganisms of cryoconite holes (algae, Archaea, bacteria, cyanobacteria, fungi, and Protista): a review
4
2016
... 冰川表面的微生物群落通过与环境的相互作用,对冰川反照率和冰川融化速率存在显著影响[7-8].冰尘是冰川表面微生物重要的栖息地[9-11],冰尘中的微生物群落主要包括藻类、古细菌、细菌、真菌、原生生物和病毒[11],细菌群落以蓝藻、绿塑菌、变形菌门、拟杆菌门和放线菌门为主[12].冰尘中的微生物在利用溶解性有机质(DOM)的同时会不断产生新的DOM[13].冰川表面DOM通过冰川融水被重新分配到其他环境,为营养匮乏的冰川环境提供营养和能量来源[14].因此,冰尘在冰川物质能量平衡、冰川生物地球化学循环特别是碳循环中发挥着重要作用.有研究表明,在极地冰川表面DOM循环过程中,光化学过程和生物过程之间存在着相互作用的关系[15].一方面,光降解可导致DOM完全氧化为CO2或部分氧化形成新的DOM,导致DOM化学组成发生改变[16-18];另一方面,冰川表面强烈的紫外辐射会伤害微生物细胞,改变微生物的活动和群落组成[19],从而显著改变DOM的化学组成[20].因此,分析山地冰川表面冰尘中DOM的“光-生物”演化过程对研究消融期山地冰川表面DOM的演化过程至关重要. ...
... [11],细菌群落以蓝藻、绿塑菌、变形菌门、拟杆菌门和放线菌门为主[12].冰尘中的微生物在利用溶解性有机质(DOM)的同时会不断产生新的DOM[13].冰川表面DOM通过冰川融水被重新分配到其他环境,为营养匮乏的冰川环境提供营养和能量来源[14].因此,冰尘在冰川物质能量平衡、冰川生物地球化学循环特别是碳循环中发挥着重要作用.有研究表明,在极地冰川表面DOM循环过程中,光化学过程和生物过程之间存在着相互作用的关系[15].一方面,光降解可导致DOM完全氧化为CO2或部分氧化形成新的DOM,导致DOM化学组成发生改变[16-18];另一方面,冰川表面强烈的紫外辐射会伤害微生物细胞,改变微生物的活动和群落组成[19],从而显著改变DOM的化学组成[20].因此,分析山地冰川表面冰尘中DOM的“光-生物”演化过程对研究消融期山地冰川表面DOM的演化过程至关重要. ...
... 有研究表明,冰尘是冰川表面微生物重要的聚集区[9-11],冰尘中微生物群落非常丰富[11].结合老虎沟12号冰川新鲜冰尘中DOM脂类(25.88%)和多肽类(20.11%)的含量,以及新鲜冰尘DOM的光谱斜率的比值SR=1.93(SR>1),说明新鲜冰尘中DOM主要源自冰尘内部的微生物活动[41,54].同时,老虎沟12号冰川地处干旱和半干旱环绕区,西边是塔里木盆地的塔克拉玛干沙漠,西南与柴达木盆地毗邻,北部是大面积的戈壁沙漠[55],因此,陆源性输入也是冰尘中DOM的重要来源,主要体现在新鲜冰尘中含有大量的低氧碳比的不饱和烃类(31.83%)和高氧碳比的不饱和烃类(18.12%),包括木质素以及单宁类化合物[56]通过风媒或干湿沉降传输到冰川表面. ...
... [11].结合老虎沟12号冰川新鲜冰尘中DOM脂类(25.88%)和多肽类(20.11%)的含量,以及新鲜冰尘DOM的光谱斜率的比值SR=1.93(SR>1),说明新鲜冰尘中DOM主要源自冰尘内部的微生物活动[41,54].同时,老虎沟12号冰川地处干旱和半干旱环绕区,西边是塔里木盆地的塔克拉玛干沙漠,西南与柴达木盆地毗邻,北部是大面积的戈壁沙漠[55],因此,陆源性输入也是冰尘中DOM的重要来源,主要体现在新鲜冰尘中含有大量的低氧碳比的不饱和烃类(31.83%)和高氧碳比的不饱和烃类(18.12%),包括木质素以及单宁类化合物[56]通过风媒或干湿沉降传输到冰川表面. ...
Biogeography of cryoconite bacterial communities on glaciers of the Tibetan Plateau
1
2017
... 冰川表面的微生物群落通过与环境的相互作用,对冰川反照率和冰川融化速率存在显著影响[7-8].冰尘是冰川表面微生物重要的栖息地[9-11],冰尘中的微生物群落主要包括藻类、古细菌、细菌、真菌、原生生物和病毒[11],细菌群落以蓝藻、绿塑菌、变形菌门、拟杆菌门和放线菌门为主[12].冰尘中的微生物在利用溶解性有机质(DOM)的同时会不断产生新的DOM[13].冰川表面DOM通过冰川融水被重新分配到其他环境,为营养匮乏的冰川环境提供营养和能量来源[14].因此,冰尘在冰川物质能量平衡、冰川生物地球化学循环特别是碳循环中发挥着重要作用.有研究表明,在极地冰川表面DOM循环过程中,光化学过程和生物过程之间存在着相互作用的关系[15].一方面,光降解可导致DOM完全氧化为CO2或部分氧化形成新的DOM,导致DOM化学组成发生改变[16-18];另一方面,冰川表面强烈的紫外辐射会伤害微生物细胞,改变微生物的活动和群落组成[19],从而显著改变DOM的化学组成[20].因此,分析山地冰川表面冰尘中DOM的“光-生物”演化过程对研究消融期山地冰川表面DOM的演化过程至关重要. ...
Do cryoconite holes have the potential to be significant sources of C, N, and P to downstream depauperate ecosystems of Taylor Valley, Antarctica?
1
2013
... 冰川表面的微生物群落通过与环境的相互作用,对冰川反照率和冰川融化速率存在显著影响[7-8].冰尘是冰川表面微生物重要的栖息地[9-11],冰尘中的微生物群落主要包括藻类、古细菌、细菌、真菌、原生生物和病毒[11],细菌群落以蓝藻、绿塑菌、变形菌门、拟杆菌门和放线菌门为主[12].冰尘中的微生物在利用溶解性有机质(DOM)的同时会不断产生新的DOM[13].冰川表面DOM通过冰川融水被重新分配到其他环境,为营养匮乏的冰川环境提供营养和能量来源[14].因此,冰尘在冰川物质能量平衡、冰川生物地球化学循环特别是碳循环中发挥着重要作用.有研究表明,在极地冰川表面DOM循环过程中,光化学过程和生物过程之间存在着相互作用的关系[15].一方面,光降解可导致DOM完全氧化为CO2或部分氧化形成新的DOM,导致DOM化学组成发生改变[16-18];另一方面,冰川表面强烈的紫外辐射会伤害微生物细胞,改变微生物的活动和群落组成[19],从而显著改变DOM的化学组成[20].因此,分析山地冰川表面冰尘中DOM的“光-生物”演化过程对研究消融期山地冰川表面DOM的演化过程至关重要. ...
Storage and release of organic carbon from glaciers and ice sheets
1
2015
... 冰川表面的微生物群落通过与环境的相互作用,对冰川反照率和冰川融化速率存在显著影响[7-8].冰尘是冰川表面微生物重要的栖息地[9-11],冰尘中的微生物群落主要包括藻类、古细菌、细菌、真菌、原生生物和病毒[11],细菌群落以蓝藻、绿塑菌、变形菌门、拟杆菌门和放线菌门为主[12].冰尘中的微生物在利用溶解性有机质(DOM)的同时会不断产生新的DOM[13].冰川表面DOM通过冰川融水被重新分配到其他环境,为营养匮乏的冰川环境提供营养和能量来源[14].因此,冰尘在冰川物质能量平衡、冰川生物地球化学循环特别是碳循环中发挥着重要作用.有研究表明,在极地冰川表面DOM循环过程中,光化学过程和生物过程之间存在着相互作用的关系[15].一方面,光降解可导致DOM完全氧化为CO2或部分氧化形成新的DOM,导致DOM化学组成发生改变[16-18];另一方面,冰川表面强烈的紫外辐射会伤害微生物细胞,改变微生物的活动和群落组成[19],从而显著改变DOM的化学组成[20].因此,分析山地冰川表面冰尘中DOM的“光-生物”演化过程对研究消融期山地冰川表面DOM的演化过程至关重要. ...
Photo-biochemical transformation of dissolved organic matter on the surface of the coastal East Antarctic ice sheet
2
2018
... 冰川表面的微生物群落通过与环境的相互作用,对冰川反照率和冰川融化速率存在显著影响[7-8].冰尘是冰川表面微生物重要的栖息地[9-11],冰尘中的微生物群落主要包括藻类、古细菌、细菌、真菌、原生生物和病毒[11],细菌群落以蓝藻、绿塑菌、变形菌门、拟杆菌门和放线菌门为主[12].冰尘中的微生物在利用溶解性有机质(DOM)的同时会不断产生新的DOM[13].冰川表面DOM通过冰川融水被重新分配到其他环境,为营养匮乏的冰川环境提供营养和能量来源[14].因此,冰尘在冰川物质能量平衡、冰川生物地球化学循环特别是碳循环中发挥着重要作用.有研究表明,在极地冰川表面DOM循环过程中,光化学过程和生物过程之间存在着相互作用的关系[15].一方面,光降解可导致DOM完全氧化为CO2或部分氧化形成新的DOM,导致DOM化学组成发生改变[16-18];另一方面,冰川表面强烈的紫外辐射会伤害微生物细胞,改变微生物的活动和群落组成[19],从而显著改变DOM的化学组成[20].因此,分析山地冰川表面冰尘中DOM的“光-生物”演化过程对研究消融期山地冰川表面DOM的演化过程至关重要. ...
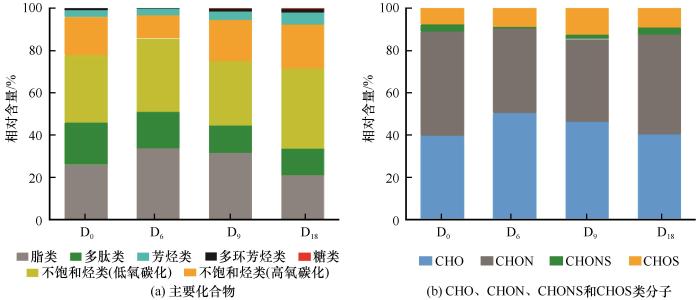
... 随着培养时间的增加,DOM分子中CHO、CHON和CHOS类分子相对含量均发生了变化[表3,图4(b)],CHONS类分子含量较少变化规律不明显.从D0至D6,总分子数从3 714减少到3 102,CHO类分子组成从39.69%升高到50.39%,CHOS类分子从7.75%升高至9.51%,CHON类分子则从49.30%减少到40.10%,从D6至D18,总分子数从3 102增加到4 500,CHO类分子含量从50.39%降低到40.47%,CHON类分子则从40.10%升高到47.16%,CHOS类分子含量变化不大.总体来说,培养初期(D0至D6),生物活性较高的CHON类分子含量迅速减少,CHO类分子和CHOS类分子含量增加;随着培养时间的增加(D6至D18),CHO类分子组成减少,CHON类分子和CHOS类分子组成增加.有研究表明光照条件下微生物活动可以对冰川表面的DOM的分子组成进行修饰,使DOM分子中的N、S、P等元素含量增加[15].因此,说明冰尘培养过程中“光-生物”演化过程使得冰尘中CHO类DOM向CHON和CHOS类DOM转化. ...
Chemical characteristics of fulvic acids from Arctic surface waters: Microbial contributions and photochemical transformations
1
2007
... 冰川表面的微生物群落通过与环境的相互作用,对冰川反照率和冰川融化速率存在显著影响[7-8].冰尘是冰川表面微生物重要的栖息地[9-11],冰尘中的微生物群落主要包括藻类、古细菌、细菌、真菌、原生生物和病毒[11],细菌群落以蓝藻、绿塑菌、变形菌门、拟杆菌门和放线菌门为主[12].冰尘中的微生物在利用溶解性有机质(DOM)的同时会不断产生新的DOM[13].冰川表面DOM通过冰川融水被重新分配到其他环境,为营养匮乏的冰川环境提供营养和能量来源[14].因此,冰尘在冰川物质能量平衡、冰川生物地球化学循环特别是碳循环中发挥着重要作用.有研究表明,在极地冰川表面DOM循环过程中,光化学过程和生物过程之间存在着相互作用的关系[15].一方面,光降解可导致DOM完全氧化为CO2或部分氧化形成新的DOM,导致DOM化学组成发生改变[16-18];另一方面,冰川表面强烈的紫外辐射会伤害微生物细胞,改变微生物的活动和群落组成[19],从而显著改变DOM的化学组成[20].因此,分析山地冰川表面冰尘中DOM的“光-生物”演化过程对研究消融期山地冰川表面DOM的演化过程至关重要. ...
Photodegradation of dissolved organic matter in forested streams of the northern Great Lakes region
0
2007
Illuminated darkness: Molecular signatures of Congo River dissolved organic matter and its photochemical alteration as revealed by ultrahigh precision mass spectrometry
1
2010
... 冰川表面的微生物群落通过与环境的相互作用,对冰川反照率和冰川融化速率存在显著影响[7-8].冰尘是冰川表面微生物重要的栖息地[9-11],冰尘中的微生物群落主要包括藻类、古细菌、细菌、真菌、原生生物和病毒[11],细菌群落以蓝藻、绿塑菌、变形菌门、拟杆菌门和放线菌门为主[12].冰尘中的微生物在利用溶解性有机质(DOM)的同时会不断产生新的DOM[13].冰川表面DOM通过冰川融水被重新分配到其他环境,为营养匮乏的冰川环境提供营养和能量来源[14].因此,冰尘在冰川物质能量平衡、冰川生物地球化学循环特别是碳循环中发挥着重要作用.有研究表明,在极地冰川表面DOM循环过程中,光化学过程和生物过程之间存在着相互作用的关系[15].一方面,光降解可导致DOM完全氧化为CO2或部分氧化形成新的DOM,导致DOM化学组成发生改变[16-18];另一方面,冰川表面强烈的紫外辐射会伤害微生物细胞,改变微生物的活动和群落组成[19],从而显著改变DOM的化学组成[20].因此,分析山地冰川表面冰尘中DOM的“光-生物”演化过程对研究消融期山地冰川表面DOM的演化过程至关重要. ...
Response of Antarctic cryoconite microbial communities to light
2
2016
... 冰川表面的微生物群落通过与环境的相互作用,对冰川反照率和冰川融化速率存在显著影响[7-8].冰尘是冰川表面微生物重要的栖息地[9-11],冰尘中的微生物群落主要包括藻类、古细菌、细菌、真菌、原生生物和病毒[11],细菌群落以蓝藻、绿塑菌、变形菌门、拟杆菌门和放线菌门为主[12].冰尘中的微生物在利用溶解性有机质(DOM)的同时会不断产生新的DOM[13].冰川表面DOM通过冰川融水被重新分配到其他环境,为营养匮乏的冰川环境提供营养和能量来源[14].因此,冰尘在冰川物质能量平衡、冰川生物地球化学循环特别是碳循环中发挥着重要作用.有研究表明,在极地冰川表面DOM循环过程中,光化学过程和生物过程之间存在着相互作用的关系[15].一方面,光降解可导致DOM完全氧化为CO2或部分氧化形成新的DOM,导致DOM化学组成发生改变[16-18];另一方面,冰川表面强烈的紫外辐射会伤害微生物细胞,改变微生物的活动和群落组成[19],从而显著改变DOM的化学组成[20].因此,分析山地冰川表面冰尘中DOM的“光-生物”演化过程对研究消融期山地冰川表面DOM的演化过程至关重要. ...
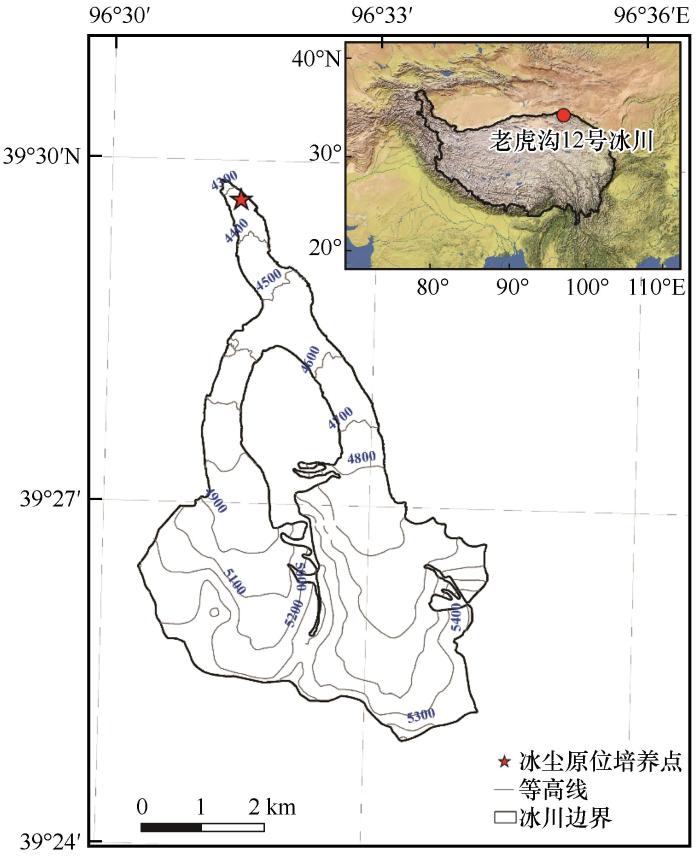
... 冰尘的原位培养过程中,随着培养时间的增加,冰尘水样中DOC浓度呈现先降低后升高的变化趋势[图2(a)],新鲜冰尘DOC的浓度为13.41 mg∙L-1(D0),培养6 d后显著降低至4.47 mg∙L-1(D6)(P<0.05),培养9 d后升高至4.95 mg∙L-1(D9),培养结束持续升高至6.71 mg∙L-1(D18)(P>0.05).培养初期(D0至D6),由于新鲜冰尘中存在大量生物活性高的DOC,沥出到冰尘水样中被微生物群落快速消耗利用[48],同时部分DOC在强烈的光照作用下发生光降解[49],导致冰尘水样中DOC浓度短期内显著降低.培养中后期(D6至D18),冰尘在培养过程中DOC生物可利用性逐渐降低,冰尘水环境中沥出的生物活性较低的DOC逐渐富集;冰尘中的自养型微生物在适应培养环境后,不断将无机碳转化成有机碳[19],释放到周围的水环境中,导致培养后期冰尘水样中DOC浓度持续升高. ...
Photochemical alteration of organic carbon draining permafrost soils shifts microbial metabolic pathways and stimulates respiration
1
2017
... 冰川表面的微生物群落通过与环境的相互作用,对冰川反照率和冰川融化速率存在显著影响[7-8].冰尘是冰川表面微生物重要的栖息地[9-11],冰尘中的微生物群落主要包括藻类、古细菌、细菌、真菌、原生生物和病毒[11],细菌群落以蓝藻、绿塑菌、变形菌门、拟杆菌门和放线菌门为主[12].冰尘中的微生物在利用溶解性有机质(DOM)的同时会不断产生新的DOM[13].冰川表面DOM通过冰川融水被重新分配到其他环境,为营养匮乏的冰川环境提供营养和能量来源[14].因此,冰尘在冰川物质能量平衡、冰川生物地球化学循环特别是碳循环中发挥着重要作用.有研究表明,在极地冰川表面DOM循环过程中,光化学过程和生物过程之间存在着相互作用的关系[15].一方面,光降解可导致DOM完全氧化为CO2或部分氧化形成新的DOM,导致DOM化学组成发生改变[16-18];另一方面,冰川表面强烈的紫外辐射会伤害微生物细胞,改变微生物的活动和群落组成[19],从而显著改变DOM的化学组成[20].因此,分析山地冰川表面冰尘中DOM的“光-生物”演化过程对研究消融期山地冰川表面DOM的演化过程至关重要. ...
Characterizing aquatic dissolved organic matter. Environ. 466
1
2003
... DOM作为一类具有复杂组成、结构和环境行为的有机混合物,通常被定义为能够通过孔径为0.45 μm滤膜且可溶于水的碳基有机化合物,是由蛋白质、油脂、类脂、碳水化合物、氨基酸以及有机酸等经过氢键、疏水等作用形成的连续统一体[21].冰川中的DOM化学组成丰富(包含有C、N、S和P等营养元素)是冰川表面生态系统中能量循环与物质循环的重要组成部分,与冰川生态系统的营养水平、化学特征以及生态结构等密切相关[22].传统的DOM分析方法主要有离子交换树脂法、核磁共振、红外光谱等,这些分析方法尽管能得到DOM的部分生物化学信息,但是存在一定的局限性.随着光谱技术和仪器分析技术的发展,紫外可见吸收光谱、三维荧光光谱由于其高灵敏性、高精度,操作简便等特性,目前被广泛应用在DOM的研究中[23-26].另外,在分子层面,傅立叶离子回旋共振质谱(FT-ICR MS)与电喷雾离子化(ESI)的结合为DOM的分析研究带来了突破性的进展,并已经广泛应用于各类水体中DOM的组成和来源分析中[27-30],FT-ICR MS的超高分辨率和分子量精确度保证了质谱峰的有效分辨以及复杂化合物的分子组成确定[31-32],为分析冰川DOM的组成和来源提供了保障.目前的研究发现,山地冰川表面冰尘和雪冰样品中DOM的主要组成是脂类和蛋白质类物质,来源主要是微生物来源,冰川中的DOM具有很高的生物可利用性[33-34].同时冰川表面的消融过程在消融初期会引起冰川表面雪冰中DOM的减少,消融后期引起含N类DOM的增多和富集,消融过程可以显著增加雪冰中DOM的生物可利用性[35].但是,目前仍缺乏对山地冰川表面DOM的“光-生物”演化过程的研究,因此本研究通过在老虎沟12号冰川消融区开展光照条件下冰尘的原位培养实验来探讨冰川表面DOM的“光-生物”演化过程,为研究冰川表面DOM的演化过程提供参考. ...
Watershed glacier coverage influences dissolved organic matter biogeochemistry in coastal watersheds of southeast Alaska
1
2014
... DOM作为一类具有复杂组成、结构和环境行为的有机混合物,通常被定义为能够通过孔径为0.45 μm滤膜且可溶于水的碳基有机化合物,是由蛋白质、油脂、类脂、碳水化合物、氨基酸以及有机酸等经过氢键、疏水等作用形成的连续统一体[21].冰川中的DOM化学组成丰富(包含有C、N、S和P等营养元素)是冰川表面生态系统中能量循环与物质循环的重要组成部分,与冰川生态系统的营养水平、化学特征以及生态结构等密切相关[22].传统的DOM分析方法主要有离子交换树脂法、核磁共振、红外光谱等,这些分析方法尽管能得到DOM的部分生物化学信息,但是存在一定的局限性.随着光谱技术和仪器分析技术的发展,紫外可见吸收光谱、三维荧光光谱由于其高灵敏性、高精度,操作简便等特性,目前被广泛应用在DOM的研究中[23-26].另外,在分子层面,傅立叶离子回旋共振质谱(FT-ICR MS)与电喷雾离子化(ESI)的结合为DOM的分析研究带来了突破性的进展,并已经广泛应用于各类水体中DOM的组成和来源分析中[27-30],FT-ICR MS的超高分辨率和分子量精确度保证了质谱峰的有效分辨以及复杂化合物的分子组成确定[31-32],为分析冰川DOM的组成和来源提供了保障.目前的研究发现,山地冰川表面冰尘和雪冰样品中DOM的主要组成是脂类和蛋白质类物质,来源主要是微生物来源,冰川中的DOM具有很高的生物可利用性[33-34].同时冰川表面的消融过程在消融初期会引起冰川表面雪冰中DOM的减少,消融后期引起含N类DOM的增多和富集,消融过程可以显著增加雪冰中DOM的生物可利用性[35].但是,目前仍缺乏对山地冰川表面DOM的“光-生物”演化过程的研究,因此本研究通过在老虎沟12号冰川消融区开展光照条件下冰尘的原位培养实验来探讨冰川表面DOM的“光-生物”演化过程,为研究冰川表面DOM的演化过程提供参考. ...
Carbonaceous species and humic like substances (HULIS) in Arctic snowpack during OASIS field campaign in Barrow
1
2012
... DOM作为一类具有复杂组成、结构和环境行为的有机混合物,通常被定义为能够通过孔径为0.45 μm滤膜且可溶于水的碳基有机化合物,是由蛋白质、油脂、类脂、碳水化合物、氨基酸以及有机酸等经过氢键、疏水等作用形成的连续统一体[21].冰川中的DOM化学组成丰富(包含有C、N、S和P等营养元素)是冰川表面生态系统中能量循环与物质循环的重要组成部分,与冰川生态系统的营养水平、化学特征以及生态结构等密切相关[22].传统的DOM分析方法主要有离子交换树脂法、核磁共振、红外光谱等,这些分析方法尽管能得到DOM的部分生物化学信息,但是存在一定的局限性.随着光谱技术和仪器分析技术的发展,紫外可见吸收光谱、三维荧光光谱由于其高灵敏性、高精度,操作简便等特性,目前被广泛应用在DOM的研究中[23-26].另外,在分子层面,傅立叶离子回旋共振质谱(FT-ICR MS)与电喷雾离子化(ESI)的结合为DOM的分析研究带来了突破性的进展,并已经广泛应用于各类水体中DOM的组成和来源分析中[27-30],FT-ICR MS的超高分辨率和分子量精确度保证了质谱峰的有效分辨以及复杂化合物的分子组成确定[31-32],为分析冰川DOM的组成和来源提供了保障.目前的研究发现,山地冰川表面冰尘和雪冰样品中DOM的主要组成是脂类和蛋白质类物质,来源主要是微生物来源,冰川中的DOM具有很高的生物可利用性[33-34].同时冰川表面的消融过程在消融初期会引起冰川表面雪冰中DOM的减少,消融后期引起含N类DOM的增多和富集,消融过程可以显著增加雪冰中DOM的生物可利用性[35].但是,目前仍缺乏对山地冰川表面DOM的“光-生物”演化过程的研究,因此本研究通过在老虎沟12号冰川消融区开展光照条件下冰尘的原位培养实验来探讨冰川表面DOM的“光-生物”演化过程,为研究冰川表面DOM的演化过程提供参考. ...
UV spectroscopy: a tool for monitoring humification and for proposing an index of the maturity of compost
0
2004
Utilization of UV-Vis spectroscopy and related data analyses for dissolved organic matter (DOM) studies: a review
0
2017
Using synchronous fluorescence spectroscopy and principal components analysis to monitor dissolved organic matter dynamics in a glacier system
1
2009
... DOM作为一类具有复杂组成、结构和环境行为的有机混合物,通常被定义为能够通过孔径为0.45 μm滤膜且可溶于水的碳基有机化合物,是由蛋白质、油脂、类脂、碳水化合物、氨基酸以及有机酸等经过氢键、疏水等作用形成的连续统一体[21].冰川中的DOM化学组成丰富(包含有C、N、S和P等营养元素)是冰川表面生态系统中能量循环与物质循环的重要组成部分,与冰川生态系统的营养水平、化学特征以及生态结构等密切相关[22].传统的DOM分析方法主要有离子交换树脂法、核磁共振、红外光谱等,这些分析方法尽管能得到DOM的部分生物化学信息,但是存在一定的局限性.随着光谱技术和仪器分析技术的发展,紫外可见吸收光谱、三维荧光光谱由于其高灵敏性、高精度,操作简便等特性,目前被广泛应用在DOM的研究中[23-26].另外,在分子层面,傅立叶离子回旋共振质谱(FT-ICR MS)与电喷雾离子化(ESI)的结合为DOM的分析研究带来了突破性的进展,并已经广泛应用于各类水体中DOM的组成和来源分析中[27-30],FT-ICR MS的超高分辨率和分子量精确度保证了质谱峰的有效分辨以及复杂化合物的分子组成确定[31-32],为分析冰川DOM的组成和来源提供了保障.目前的研究发现,山地冰川表面冰尘和雪冰样品中DOM的主要组成是脂类和蛋白质类物质,来源主要是微生物来源,冰川中的DOM具有很高的生物可利用性[33-34].同时冰川表面的消融过程在消融初期会引起冰川表面雪冰中DOM的减少,消融后期引起含N类DOM的增多和富集,消融过程可以显著增加雪冰中DOM的生物可利用性[35].但是,目前仍缺乏对山地冰川表面DOM的“光-生物”演化过程的研究,因此本研究通过在老虎沟12号冰川消融区开展光照条件下冰尘的原位培养实验来探讨冰川表面DOM的“光-生物”演化过程,为研究冰川表面DOM的演化过程提供参考. ...
Molecular insights on dissolved organic matter transformation by supraglacial microbial communities
1
2017
... DOM作为一类具有复杂组成、结构和环境行为的有机混合物,通常被定义为能够通过孔径为0.45 μm滤膜且可溶于水的碳基有机化合物,是由蛋白质、油脂、类脂、碳水化合物、氨基酸以及有机酸等经过氢键、疏水等作用形成的连续统一体[21].冰川中的DOM化学组成丰富(包含有C、N、S和P等营养元素)是冰川表面生态系统中能量循环与物质循环的重要组成部分,与冰川生态系统的营养水平、化学特征以及生态结构等密切相关[22].传统的DOM分析方法主要有离子交换树脂法、核磁共振、红外光谱等,这些分析方法尽管能得到DOM的部分生物化学信息,但是存在一定的局限性.随着光谱技术和仪器分析技术的发展,紫外可见吸收光谱、三维荧光光谱由于其高灵敏性、高精度,操作简便等特性,目前被广泛应用在DOM的研究中[23-26].另外,在分子层面,傅立叶离子回旋共振质谱(FT-ICR MS)与电喷雾离子化(ESI)的结合为DOM的分析研究带来了突破性的进展,并已经广泛应用于各类水体中DOM的组成和来源分析中[27-30],FT-ICR MS的超高分辨率和分子量精确度保证了质谱峰的有效分辨以及复杂化合物的分子组成确定[31-32],为分析冰川DOM的组成和来源提供了保障.目前的研究发现,山地冰川表面冰尘和雪冰样品中DOM的主要组成是脂类和蛋白质类物质,来源主要是微生物来源,冰川中的DOM具有很高的生物可利用性[33-34].同时冰川表面的消融过程在消融初期会引起冰川表面雪冰中DOM的减少,消融后期引起含N类DOM的增多和富集,消融过程可以显著增加雪冰中DOM的生物可利用性[35].但是,目前仍缺乏对山地冰川表面DOM的“光-生物”演化过程的研究,因此本研究通过在老虎沟12号冰川消融区开展光照条件下冰尘的原位培养实验来探讨冰川表面DOM的“光-生物”演化过程,为研究冰川表面DOM的演化过程提供参考. ...
Ultrahigh resolution mass spectrometric differentiation of dissolved organic matter isolated by coupled reverse osmosis-electrodialysis from various major oceanic water masses
0
2014
Molecular characterization of organic aerosol in the Himalayas: insight from ultra-high-resolution mass spectrometry
0
2019
Characterization of dissolved organic matter from a Greenland ice core by nanospray ionization Fourier transform ion cyclotron resonance mass spectrometry
1
2013
... DOM作为一类具有复杂组成、结构和环境行为的有机混合物,通常被定义为能够通过孔径为0.45 μm滤膜且可溶于水的碳基有机化合物,是由蛋白质、油脂、类脂、碳水化合物、氨基酸以及有机酸等经过氢键、疏水等作用形成的连续统一体[21].冰川中的DOM化学组成丰富(包含有C、N、S和P等营养元素)是冰川表面生态系统中能量循环与物质循环的重要组成部分,与冰川生态系统的营养水平、化学特征以及生态结构等密切相关[22].传统的DOM分析方法主要有离子交换树脂法、核磁共振、红外光谱等,这些分析方法尽管能得到DOM的部分生物化学信息,但是存在一定的局限性.随着光谱技术和仪器分析技术的发展,紫外可见吸收光谱、三维荧光光谱由于其高灵敏性、高精度,操作简便等特性,目前被广泛应用在DOM的研究中[23-26].另外,在分子层面,傅立叶离子回旋共振质谱(FT-ICR MS)与电喷雾离子化(ESI)的结合为DOM的分析研究带来了突破性的进展,并已经广泛应用于各类水体中DOM的组成和来源分析中[27-30],FT-ICR MS的超高分辨率和分子量精确度保证了质谱峰的有效分辨以及复杂化合物的分子组成确定[31-32],为分析冰川DOM的组成和来源提供了保障.目前的研究发现,山地冰川表面冰尘和雪冰样品中DOM的主要组成是脂类和蛋白质类物质,来源主要是微生物来源,冰川中的DOM具有很高的生物可利用性[33-34].同时冰川表面的消融过程在消融初期会引起冰川表面雪冰中DOM的减少,消融后期引起含N类DOM的增多和富集,消融过程可以显著增加雪冰中DOM的生物可利用性[35].但是,目前仍缺乏对山地冰川表面DOM的“光-生物”演化过程的研究,因此本研究通过在老虎沟12号冰川消融区开展光照条件下冰尘的原位培养实验来探讨冰川表面DOM的“光-生物”演化过程,为研究冰川表面DOM的演化过程提供参考. ...
Dynamic range and mass accuracy of wide-scan direct infusion nanoelectrospray Fourier transform ion cyclotron resonance mass spectrometry-based metabolomics increased by the spectral stitching method
1
2007
... DOM作为一类具有复杂组成、结构和环境行为的有机混合物,通常被定义为能够通过孔径为0.45 μm滤膜且可溶于水的碳基有机化合物,是由蛋白质、油脂、类脂、碳水化合物、氨基酸以及有机酸等经过氢键、疏水等作用形成的连续统一体[21].冰川中的DOM化学组成丰富(包含有C、N、S和P等营养元素)是冰川表面生态系统中能量循环与物质循环的重要组成部分,与冰川生态系统的营养水平、化学特征以及生态结构等密切相关[22].传统的DOM分析方法主要有离子交换树脂法、核磁共振、红外光谱等,这些分析方法尽管能得到DOM的部分生物化学信息,但是存在一定的局限性.随着光谱技术和仪器分析技术的发展,紫外可见吸收光谱、三维荧光光谱由于其高灵敏性、高精度,操作简便等特性,目前被广泛应用在DOM的研究中[23-26].另外,在分子层面,傅立叶离子回旋共振质谱(FT-ICR MS)与电喷雾离子化(ESI)的结合为DOM的分析研究带来了突破性的进展,并已经广泛应用于各类水体中DOM的组成和来源分析中[27-30],FT-ICR MS的超高分辨率和分子量精确度保证了质谱峰的有效分辨以及复杂化合物的分子组成确定[31-32],为分析冰川DOM的组成和来源提供了保障.目前的研究发现,山地冰川表面冰尘和雪冰样品中DOM的主要组成是脂类和蛋白质类物质,来源主要是微生物来源,冰川中的DOM具有很高的生物可利用性[33-34].同时冰川表面的消融过程在消融初期会引起冰川表面雪冰中DOM的减少,消融后期引起含N类DOM的增多和富集,消融过程可以显著增加雪冰中DOM的生物可利用性[35].但是,目前仍缺乏对山地冰川表面DOM的“光-生物”演化过程的研究,因此本研究通过在老虎沟12号冰川消融区开展光照条件下冰尘的原位培养实验来探讨冰川表面DOM的“光-生物”演化过程,为研究冰川表面DOM的演化过程提供参考. ...
Establishing a measure of reproducibility of ultrahigh-resolution mass spectra for complex mixtures of natural organic matter
1
2012
... DOM作为一类具有复杂组成、结构和环境行为的有机混合物,通常被定义为能够通过孔径为0.45 μm滤膜且可溶于水的碳基有机化合物,是由蛋白质、油脂、类脂、碳水化合物、氨基酸以及有机酸等经过氢键、疏水等作用形成的连续统一体[21].冰川中的DOM化学组成丰富(包含有C、N、S和P等营养元素)是冰川表面生态系统中能量循环与物质循环的重要组成部分,与冰川生态系统的营养水平、化学特征以及生态结构等密切相关[22].传统的DOM分析方法主要有离子交换树脂法、核磁共振、红外光谱等,这些分析方法尽管能得到DOM的部分生物化学信息,但是存在一定的局限性.随着光谱技术和仪器分析技术的发展,紫外可见吸收光谱、三维荧光光谱由于其高灵敏性、高精度,操作简便等特性,目前被广泛应用在DOM的研究中[23-26].另外,在分子层面,傅立叶离子回旋共振质谱(FT-ICR MS)与电喷雾离子化(ESI)的结合为DOM的分析研究带来了突破性的进展,并已经广泛应用于各类水体中DOM的组成和来源分析中[27-30],FT-ICR MS的超高分辨率和分子量精确度保证了质谱峰的有效分辨以及复杂化合物的分子组成确定[31-32],为分析冰川DOM的组成和来源提供了保障.目前的研究发现,山地冰川表面冰尘和雪冰样品中DOM的主要组成是脂类和蛋白质类物质,来源主要是微生物来源,冰川中的DOM具有很高的生物可利用性[33-34].同时冰川表面的消融过程在消融初期会引起冰川表面雪冰中DOM的减少,消融后期引起含N类DOM的增多和富集,消融过程可以显著增加雪冰中DOM的生物可利用性[35].但是,目前仍缺乏对山地冰川表面DOM的“光-生物”演化过程的研究,因此本研究通过在老虎沟12号冰川消融区开展光照条件下冰尘的原位培养实验来探讨冰川表面DOM的“光-生物”演化过程,为研究冰川表面DOM的演化过程提供参考. ...
Chemical composition of microbe-derived dissolved organic matter in cryoconite in Tibetan Plateau glaciers: insights from Fourier transform ion cyclotron resonance mass spectrometry analysis
1
2016
... DOM作为一类具有复杂组成、结构和环境行为的有机混合物,通常被定义为能够通过孔径为0.45 μm滤膜且可溶于水的碳基有机化合物,是由蛋白质、油脂、类脂、碳水化合物、氨基酸以及有机酸等经过氢键、疏水等作用形成的连续统一体[21].冰川中的DOM化学组成丰富(包含有C、N、S和P等营养元素)是冰川表面生态系统中能量循环与物质循环的重要组成部分,与冰川生态系统的营养水平、化学特征以及生态结构等密切相关[22].传统的DOM分析方法主要有离子交换树脂法、核磁共振、红外光谱等,这些分析方法尽管能得到DOM的部分生物化学信息,但是存在一定的局限性.随着光谱技术和仪器分析技术的发展,紫外可见吸收光谱、三维荧光光谱由于其高灵敏性、高精度,操作简便等特性,目前被广泛应用在DOM的研究中[23-26].另外,在分子层面,傅立叶离子回旋共振质谱(FT-ICR MS)与电喷雾离子化(ESI)的结合为DOM的分析研究带来了突破性的进展,并已经广泛应用于各类水体中DOM的组成和来源分析中[27-30],FT-ICR MS的超高分辨率和分子量精确度保证了质谱峰的有效分辨以及复杂化合物的分子组成确定[31-32],为分析冰川DOM的组成和来源提供了保障.目前的研究发现,山地冰川表面冰尘和雪冰样品中DOM的主要组成是脂类和蛋白质类物质,来源主要是微生物来源,冰川中的DOM具有很高的生物可利用性[33-34].同时冰川表面的消融过程在消融初期会引起冰川表面雪冰中DOM的减少,消融后期引起含N类DOM的增多和富集,消融过程可以显著增加雪冰中DOM的生物可利用性[35].但是,目前仍缺乏对山地冰川表面DOM的“光-生物”演化过程的研究,因此本研究通过在老虎沟12号冰川消融区开展光照条件下冰尘的原位培养实验来探讨冰川表面DOM的“光-生物”演化过程,为研究冰川表面DOM的演化过程提供参考. ...
Characteristics and sources of dissolved organic matter in a glacier in the northern Tibetan Plateau: differences between different snow categories
1
2018
... DOM作为一类具有复杂组成、结构和环境行为的有机混合物,通常被定义为能够通过孔径为0.45 μm滤膜且可溶于水的碳基有机化合物,是由蛋白质、油脂、类脂、碳水化合物、氨基酸以及有机酸等经过氢键、疏水等作用形成的连续统一体[21].冰川中的DOM化学组成丰富(包含有C、N、S和P等营养元素)是冰川表面生态系统中能量循环与物质循环的重要组成部分,与冰川生态系统的营养水平、化学特征以及生态结构等密切相关[22].传统的DOM分析方法主要有离子交换树脂法、核磁共振、红外光谱等,这些分析方法尽管能得到DOM的部分生物化学信息,但是存在一定的局限性.随着光谱技术和仪器分析技术的发展,紫外可见吸收光谱、三维荧光光谱由于其高灵敏性、高精度,操作简便等特性,目前被广泛应用在DOM的研究中[23-26].另外,在分子层面,傅立叶离子回旋共振质谱(FT-ICR MS)与电喷雾离子化(ESI)的结合为DOM的分析研究带来了突破性的进展,并已经广泛应用于各类水体中DOM的组成和来源分析中[27-30],FT-ICR MS的超高分辨率和分子量精确度保证了质谱峰的有效分辨以及复杂化合物的分子组成确定[31-32],为分析冰川DOM的组成和来源提供了保障.目前的研究发现,山地冰川表面冰尘和雪冰样品中DOM的主要组成是脂类和蛋白质类物质,来源主要是微生物来源,冰川中的DOM具有很高的生物可利用性[33-34].同时冰川表面的消融过程在消融初期会引起冰川表面雪冰中DOM的减少,消融后期引起含N类DOM的增多和富集,消融过程可以显著增加雪冰中DOM的生物可利用性[35].但是,目前仍缺乏对山地冰川表面DOM的“光-生物”演化过程的研究,因此本研究通过在老虎沟12号冰川消融区开展光照条件下冰尘的原位培养实验来探讨冰川表面DOM的“光-生物”演化过程,为研究冰川表面DOM的演化过程提供参考. ...
Biochemical evolution of dissolved organic matter during snow metamorphism across the ablation season for a glacier on the central Tibetan Plateau
1
2020
... DOM作为一类具有复杂组成、结构和环境行为的有机混合物,通常被定义为能够通过孔径为0.45 μm滤膜且可溶于水的碳基有机化合物,是由蛋白质、油脂、类脂、碳水化合物、氨基酸以及有机酸等经过氢键、疏水等作用形成的连续统一体[21].冰川中的DOM化学组成丰富(包含有C、N、S和P等营养元素)是冰川表面生态系统中能量循环与物质循环的重要组成部分,与冰川生态系统的营养水平、化学特征以及生态结构等密切相关[22].传统的DOM分析方法主要有离子交换树脂法、核磁共振、红外光谱等,这些分析方法尽管能得到DOM的部分生物化学信息,但是存在一定的局限性.随着光谱技术和仪器分析技术的发展,紫外可见吸收光谱、三维荧光光谱由于其高灵敏性、高精度,操作简便等特性,目前被广泛应用在DOM的研究中[23-26].另外,在分子层面,傅立叶离子回旋共振质谱(FT-ICR MS)与电喷雾离子化(ESI)的结合为DOM的分析研究带来了突破性的进展,并已经广泛应用于各类水体中DOM的组成和来源分析中[27-30],FT-ICR MS的超高分辨率和分子量精确度保证了质谱峰的有效分辨以及复杂化合物的分子组成确定[31-32],为分析冰川DOM的组成和来源提供了保障.目前的研究发现,山地冰川表面冰尘和雪冰样品中DOM的主要组成是脂类和蛋白质类物质,来源主要是微生物来源,冰川中的DOM具有很高的生物可利用性[33-34].同时冰川表面的消融过程在消融初期会引起冰川表面雪冰中DOM的减少,消融后期引起含N类DOM的增多和富集,消融过程可以显著增加雪冰中DOM的生物可利用性[35].但是,目前仍缺乏对山地冰川表面DOM的“光-生物”演化过程的研究,因此本研究通过在老虎沟12号冰川消融区开展光照条件下冰尘的原位培养实验来探讨冰川表面DOM的“光-生物”演化过程,为研究冰川表面DOM的演化过程提供参考. ...
1958—2005年祁连山老虎沟12号冰川变化特征研究
1
2008
... 研究区域选择青藏高原北部祁连山地区老虎沟12号冰川(39°25.7′ N,96°33.4′ E,4 260~5 483 m a.s.l.),位于甘肃肃北蒙古族自治县境内.祁连山地区发育有大量的山岳冰川,是我国西北干旱区重要的“天然水库”[36].老虎沟12号冰川处于祁连山西段北坡的大雪山地区,由东西两支冰川组成,两支冰川在海拔4 550 m处汇合,是祁连山冰川中最大并且最具代表性的复式山谷冰川.最高海拔5 483 m,末端海拔4 250 m,总长9.7 km,面积20.37 km2,冰储量达1.943 km3,相比第一次冰川编目中1957年的冰川资料,面积缩小了1.54 km2,冰储量减少了0.1816 km3[37].老虎沟12号冰川消融区表面冰尘含量丰富且平缓开阔,被视为开展冰川化学和冰川消融研究的理想地点,是进行冰尘原位培养探究山地冰川表面DOM演化过程的理想区域. ...
1958—2005年祁连山老虎沟12号冰川变化特征研究
1
2008
... 研究区域选择青藏高原北部祁连山地区老虎沟12号冰川(39°25.7′ N,96°33.4′ E,4 260~5 483 m a.s.l.),位于甘肃肃北蒙古族自治县境内.祁连山地区发育有大量的山岳冰川,是我国西北干旱区重要的“天然水库”[36].老虎沟12号冰川处于祁连山西段北坡的大雪山地区,由东西两支冰川组成,两支冰川在海拔4 550 m处汇合,是祁连山冰川中最大并且最具代表性的复式山谷冰川.最高海拔5 483 m,末端海拔4 250 m,总长9.7 km,面积20.37 km2,冰储量达1.943 km3,相比第一次冰川编目中1957年的冰川资料,面积缩小了1.54 km2,冰储量减少了0.1816 km3[37].老虎沟12号冰川消融区表面冰尘含量丰富且平缓开阔,被视为开展冰川化学和冰川消融研究的理想地点,是进行冰尘原位培养探究山地冰川表面DOM演化过程的理想区域. ...
Variations of Laohugou Glacier No. 12 in the western Qilian Mountains, China, from 1957 to 2015
1
2018
... 研究区域选择青藏高原北部祁连山地区老虎沟12号冰川(39°25.7′ N,96°33.4′ E,4 260~5 483 m a.s.l.),位于甘肃肃北蒙古族自治县境内.祁连山地区发育有大量的山岳冰川,是我国西北干旱区重要的“天然水库”[36].老虎沟12号冰川处于祁连山西段北坡的大雪山地区,由东西两支冰川组成,两支冰川在海拔4 550 m处汇合,是祁连山冰川中最大并且最具代表性的复式山谷冰川.最高海拔5 483 m,末端海拔4 250 m,总长9.7 km,面积20.37 km2,冰储量达1.943 km3,相比第一次冰川编目中1957年的冰川资料,面积缩小了1.54 km2,冰储量减少了0.1816 km3[37].老虎沟12号冰川消融区表面冰尘含量丰富且平缓开阔,被视为开展冰川化学和冰川消融研究的理想地点,是进行冰尘原位培养探究山地冰川表面DOM演化过程的理想区域. ...
Dynamics of dissolved organic nitrogen and carbon in a Central European Norway spruce ecosystem
1
1999
... 将不同培养时段的冰尘水样用孔径为0.45 μm的聚四氟乙烯滤头(Pall Life Sciences, AnnArbor, MI, USA)过滤,过滤后的滤液直接用于测定溶解性有机碳(DOC)浓度和紫外可见光谱,DOM的结构组成异常复杂,基本组成元素为C、H、O、N、S、P等[38-39],由于C是DOM的最主要也是最重要的构成元素,所以通常用DOC的浓度来表征DOM的浓度.DOC浓度和紫外可见光谱分析将同一培养时段的剩余样品混合后进行固相萃取用于高分辨质谱分析. ...
Biogeochemically diverse organic matter in Alpine glaciers and its downstream fate
1
2012
... 将不同培养时段的冰尘水样用孔径为0.45 μm的聚四氟乙烯滤头(Pall Life Sciences, AnnArbor, MI, USA)过滤,过滤后的滤液直接用于测定溶解性有机碳(DOC)浓度和紫外可见光谱,DOM的结构组成异常复杂,基本组成元素为C、H、O、N、S、P等[38-39],由于C是DOM的最主要也是最重要的构成元素,所以通常用DOC的浓度来表征DOM的浓度.DOC浓度和紫外可见光谱分析将同一培养时段的剩余样品混合后进行固相萃取用于高分辨质谱分析. ...
Characteristics and sources of chromophoric dissolved organic matter in lakes of the Yungui Plateau, China, differing in trophic state and altitude
1
2010
... DOM的紫外可见吸收光谱的测定采用岛津UV-2410PC紫外可见分光光度计,以超纯水作为空白,扫描样品在190~900 nm处的吸光度值,比色皿采用5 cm的石英比色皿.样品测试完成后,通过减去690 nm至700 nm之间的平均吸光值来修正每个样品的吸光值,然后通过式(1)将吸光值转化成吸收系数[40]: ...
Absorption spectral slopes and slope ratios as indicators of molecular weight, source, and photobleaching of chromophoric dissolved organic matter
3
2008
... 式中:k为背景参数.光谱斜率比值SR是S275~295与S350~400之间的比值[41]. ...
... 分析冰尘DOM的特征紫外吸光度SUVA254发现,培养初期,冰尘中DOM的SUVA254从0.35 L∙mg∙C-1∙m-1(D0)显著降低至0.08 L∙mg∙C-1∙m-1(D6)(表2),培养后期,SUVA254显著升高至0.50 L∙mg∙C-1∙m-1(D18)(P<0.05),这一变化表明培养后期DOM中具有吸光性的化合物含量显著增加[42].光谱斜率的比值SR的数值可以在一定程度上表征有色类DOM的来源,SR>1和表示有色类DOM可能是内源性的DOM,而SR<1则表示有色类DOM可能是外源性的DOM[41].整个培养过程中,冰尘中DOM的SR从1.93(D0)显著降低至0.57(D18)(表2),表明DOM的来源逐渐由内源性来源向外源性来源转变. ...
... 有研究表明,冰尘是冰川表面微生物重要的聚集区[9-11],冰尘中微生物群落非常丰富[11].结合老虎沟12号冰川新鲜冰尘中DOM脂类(25.88%)和多肽类(20.11%)的含量,以及新鲜冰尘DOM的光谱斜率的比值SR=1.93(SR>1),说明新鲜冰尘中DOM主要源自冰尘内部的微生物活动[41,54].同时,老虎沟12号冰川地处干旱和半干旱环绕区,西边是塔里木盆地的塔克拉玛干沙漠,西南与柴达木盆地毗邻,北部是大面积的戈壁沙漠[55],因此,陆源性输入也是冰尘中DOM的重要来源,主要体现在新鲜冰尘中含有大量的低氧碳比的不饱和烃类(31.83%)和高氧碳比的不饱和烃类(18.12%),包括木质素以及单宁类化合物[56]通过风媒或干湿沉降传输到冰川表面. ...
Evaluation of specific ultraviolet absorbance as an indicator of the chemical composition and reactivity of dissolved organic carbon
2
2003
... 254 nm处的紫外吸收值SUVA254可以作为DOM不饱和程度和吸光性强弱的一个指数,SUVA254是由波长254 nm处吸光值的均值除以样品DOM的平均浓度得到的,单位为L∙mg∙C-1∙m-1[42]. ...
... 分析冰尘DOM的特征紫外吸光度SUVA254发现,培养初期,冰尘中DOM的SUVA254从0.35 L∙mg∙C-1∙m-1(D0)显著降低至0.08 L∙mg∙C-1∙m-1(D6)(表2),培养后期,SUVA254显著升高至0.50 L∙mg∙C-1∙m-1(D18)(P<0.05),这一变化表明培养后期DOM中具有吸光性的化合物含量显著增加[42].光谱斜率的比值SR的数值可以在一定程度上表征有色类DOM的来源,SR>1和表示有色类DOM可能是内源性的DOM,而SR<1则表示有色类DOM可能是外源性的DOM[41].整个培养过程中,冰尘中DOM的SR从1.93(D0)显著降低至0.57(D18)(表2),表明DOM的来源逐渐由内源性来源向外源性来源转变. ...
Predator data station: A fast data acquisition system for advanced FT-ICR MS experiments
1
2011
... 将固相萃取的样品用1 mL左右的甲醇溶解,通过ESI离子源(Bruker Daltonik GmbH, Bremen, Germany),ESI电离源正负离子模式均使用,经过电喷雾离子化的样品进入配有9.4 T的FT-ICR MS(Bruker Daltonik GmbH, Bremen, Germany)进行分析,质荷比的检测范围是150~800 Da,谱图叠加100次以提高信噪比.信噪比大于6的所有质谱峰被导入到Excel数据表中,利用美国高磁国家实验室开发的PetrOrg©™软件进行分子式计算[43].计算分子式时含有的12C、1H、16O、14N、32S、13C、18O和34S最大原子数分别设定为30、60、20、3、1、1、1和1,含有同位素(例如13C、18O和34S)的分子不纳入后续分析. ...
Graphical method for analysis of ultrahigh-resolution broadband mass spectra of natural organic matter, the van Krevelen diagram
1
2003
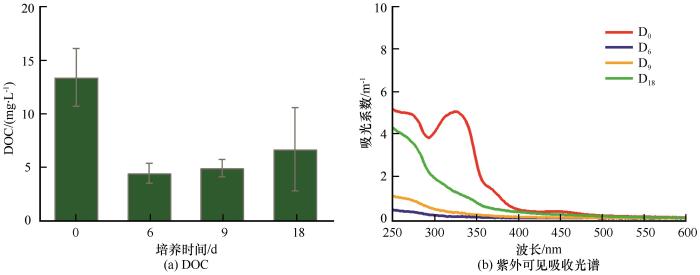
... 为了更好的对FT-ICR MS的结果进行分析,我们采用Van Krevelen图(VK图)[44],并计算了芳香性指数(modified aromaticity index, AImod)[45-46].VK图是由分子内O、C原子个数比值和H、C原子个数比值构成的二维图谱,其中O/C的值为横坐标,H/C的值为纵坐标,主要的生物化学组分(包括脂类、多肽类、不饱和烃类、芳烃类、多环芳烃类和糖类等)都具有特定的O/C和H/C,因此,在VK图中每类化合物都有其特定的位置.AImod是对DOM芳香化程度的一个度量,其计算公式为: ...
From mass to structure: An aromaticity index for high‐resolution mass data of natural organic matter
2
2006
... 为了更好的对FT-ICR MS的结果进行分析,我们采用Van Krevelen图(VK图)[44],并计算了芳香性指数(modified aromaticity index, AImod)[45-46].VK图是由分子内O、C原子个数比值和H、C原子个数比值构成的二维图谱,其中O/C的值为横坐标,H/C的值为纵坐标,主要的生物化学组分(包括脂类、多肽类、不饱和烃类、芳烃类、多环芳烃类和糖类等)都具有特定的O/C和H/C,因此,在VK图中每类化合物都有其特定的位置.AImod是对DOM芳香化程度的一个度量,其计算公式为: ...
... AImod≥0.5以及<0.67是芳香类化合物,AImod≥0.67则属于多环芳烃类化合物[45-46].本研究中用到的常见的DOM组分的化合物分类方法见下(表1)[47]. ...
Corrigendum: From mass to structure: an aromaticity index for high‐resolution mass data of natural organic matter
2
2015
... 为了更好的对FT-ICR MS的结果进行分析,我们采用Van Krevelen图(VK图)[44],并计算了芳香性指数(modified aromaticity index, AImod)[45-46].VK图是由分子内O、C原子个数比值和H、C原子个数比值构成的二维图谱,其中O/C的值为横坐标,H/C的值为纵坐标,主要的生物化学组分(包括脂类、多肽类、不饱和烃类、芳烃类、多环芳烃类和糖类等)都具有特定的O/C和H/C,因此,在VK图中每类化合物都有其特定的位置.AImod是对DOM芳香化程度的一个度量,其计算公式为: ...
... AImod≥0.5以及<0.67是芳香类化合物,AImod≥0.67则属于多环芳烃类化合物[45-46].本研究中用到的常见的DOM组分的化合物分类方法见下(表1)[47]. ...
Source and biolability of ancient dissolved organic matter in glacier and lake ecosystems on the Tibetan Plateau
3
2014
... AImod≥0.5以及<0.67是芳香类化合物,AImod≥0.67则属于多环芳烃类化合物[45-46].本研究中用到的常见的DOM组分的化合物分类方法见下(表1)[47]. ...
... 傅立叶离子回旋共振质谱(FT-ICR MS)分析得到的常见化合物类型分类[47] ...
... The classification method of compound classes used for categorizing FT-ICR MS molecular formulas[47] ...
Microbial production and consumption of dissolved organic matter in glacial ecosystems on the Tibetan Plateau
1
2019
... 冰尘的原位培养过程中,随着培养时间的增加,冰尘水样中DOC浓度呈现先降低后升高的变化趋势[图2(a)],新鲜冰尘DOC的浓度为13.41 mg∙L-1(D0),培养6 d后显著降低至4.47 mg∙L-1(D6)(P<0.05),培养9 d后升高至4.95 mg∙L-1(D9),培养结束持续升高至6.71 mg∙L-1(D18)(P>0.05).培养初期(D0至D6),由于新鲜冰尘中存在大量生物活性高的DOC,沥出到冰尘水样中被微生物群落快速消耗利用[48],同时部分DOC在强烈的光照作用下发生光降解[49],导致冰尘水样中DOC浓度短期内显著降低.培养中后期(D6至D18),冰尘在培养过程中DOC生物可利用性逐渐降低,冰尘水环境中沥出的生物活性较低的DOC逐渐富集;冰尘中的自养型微生物在适应培养环境后,不断将无机碳转化成有机碳[19],释放到周围的水环境中,导致培养后期冰尘水样中DOC浓度持续升高. ...
Molecular signatures of biogeochemical transformations in dissolved organic matter from ten world rivers
1
2016
... 冰尘的原位培养过程中,随着培养时间的增加,冰尘水样中DOC浓度呈现先降低后升高的变化趋势[图2(a)],新鲜冰尘DOC的浓度为13.41 mg∙L-1(D0),培养6 d后显著降低至4.47 mg∙L-1(D6)(P<0.05),培养9 d后升高至4.95 mg∙L-1(D9),培养结束持续升高至6.71 mg∙L-1(D18)(P>0.05).培养初期(D0至D6),由于新鲜冰尘中存在大量生物活性高的DOC,沥出到冰尘水样中被微生物群落快速消耗利用[48],同时部分DOC在强烈的光照作用下发生光降解[49],导致冰尘水样中DOC浓度短期内显著降低.培养中后期(D6至D18),冰尘在培养过程中DOC生物可利用性逐渐降低,冰尘水环境中沥出的生物活性较低的DOC逐渐富集;冰尘中的自养型微生物在适应培养环境后,不断将无机碳转化成有机碳[19],释放到周围的水环境中,导致培养后期冰尘水样中DOC浓度持续升高. ...
Spring production of mycosporine-like amino acids and other UV-absorbing compounds in sea ice-associated algae communities in the Canadian Arctic
1
2015
... 通过对不同培养时间冰尘水样中DOM的紫外可见光谱分析发现[图2(b)],新鲜冰尘(D0)中的DOM在300~350 nm范围内有明显的吸收峰,这一吸收峰是类菌孢素氨基酸类化合物(mycosporine-like amino acids,MAAs)的典型吸收峰,MAAs是生长在紫外线较强环境下的微生物(如:子囊菌类和担子菌类的真菌、蓝藻、异养细菌以及微藻类)产生的一类能保护自身细胞免受紫外线伤害的化合物,在海洋和高海拔地区的湖泊中都有发现[50-52];培养6 d后,冰尘水样中DOM在300~350 nm范围内的吸收峰消失,仅在250~400 nm处有吸收峰,且吸收值较小;培养9 d后,冰尘水样中DOM在250~400 nm之间的吸收值开始逐渐增加,培养至18 d时,冰尘水样中DOM在250~400 nm的吸收值升高;以上变化趋势表明,培养过程中冰尘水样中具有吸光性的DOM浓度呈现先降低后升高的变化趋势. ...
Mycosporine-like amino acids and related gadusols: biosynthesis, accumulation, and UV-protective functions in aquatic organisms
0
2002
Extremotrophs, extremophiles and broadband pigmentation strategies in a high arctic ice shelf ecosystem
1
2005
... 通过对不同培养时间冰尘水样中DOM的紫外可见光谱分析发现[图2(b)],新鲜冰尘(D0)中的DOM在300~350 nm范围内有明显的吸收峰,这一吸收峰是类菌孢素氨基酸类化合物(mycosporine-like amino acids,MAAs)的典型吸收峰,MAAs是生长在紫外线较强环境下的微生物(如:子囊菌类和担子菌类的真菌、蓝藻、异养细菌以及微藻类)产生的一类能保护自身细胞免受紫外线伤害的化合物,在海洋和高海拔地区的湖泊中都有发现[50-52];培养6 d后,冰尘水样中DOM在300~350 nm范围内的吸收峰消失,仅在250~400 nm处有吸收峰,且吸收值较小;培养9 d后,冰尘水样中DOM在250~400 nm之间的吸收值开始逐渐增加,培养至18 d时,冰尘水样中DOM在250~400 nm的吸收值升高;以上变化趋势表明,培养过程中冰尘水样中具有吸光性的DOM浓度呈现先降低后升高的变化趋势. ...
Indexing permafrost soil organic matter degradation using high-resolution mass spectrometry
1
2015
... ESI-FT-ICR MS结果显示(图3),老虎沟12号冰川新鲜冰尘中(D0)DOM的分子组成丰富,主要包含脂类(25.88%)、多肽类(20.11%)、低氧碳比的不饱和烃类(31.83%)和高氧碳比的不饱和烃类(18.12%),同时含有少量的芳烃类(3.34%)、多环芳烃类(0.59%)以及糖类化合物(0.13%)(表3).按照不同元素组成对冰尘中DOM的分子进行分类(表4),发现新鲜冰尘中DOM的主要分子组成是CHO类分子(39.69%)和CHON类分子(49.30%),同时含有少量的CHOS(7.75%)和CHONS(3.26%)类分子,新鲜冰尘中CHON类分子含量接近50%,说明新鲜冰尘中的DOM具有很高的生物可利用性[53]. ...
Origin and sources of dissolved organic matter in snow on the East Antarctic ice sheet
1
2014
... 有研究表明,冰尘是冰川表面微生物重要的聚集区[9-11],冰尘中微生物群落非常丰富[11].结合老虎沟12号冰川新鲜冰尘中DOM脂类(25.88%)和多肽类(20.11%)的含量,以及新鲜冰尘DOM的光谱斜率的比值SR=1.93(SR>1),说明新鲜冰尘中DOM主要源自冰尘内部的微生物活动[41,54].同时,老虎沟12号冰川地处干旱和半干旱环绕区,西边是塔里木盆地的塔克拉玛干沙漠,西南与柴达木盆地毗邻,北部是大面积的戈壁沙漠[55],因此,陆源性输入也是冰尘中DOM的重要来源,主要体现在新鲜冰尘中含有大量的低氧碳比的不饱和烃类(31.83%)和高氧碳比的不饱和烃类(18.12%),包括木质素以及单宁类化合物[56]通过风媒或干湿沉降传输到冰川表面. ...
Seasonal and diurnal variations in aerosol concentrations at a high-altitude site on the northern boundary of Qinghai-Xizang Plateau
1
2013
... 有研究表明,冰尘是冰川表面微生物重要的聚集区[9-11],冰尘中微生物群落非常丰富[11].结合老虎沟12号冰川新鲜冰尘中DOM脂类(25.88%)和多肽类(20.11%)的含量,以及新鲜冰尘DOM的光谱斜率的比值SR=1.93(SR>1),说明新鲜冰尘中DOM主要源自冰尘内部的微生物活动[41,54].同时,老虎沟12号冰川地处干旱和半干旱环绕区,西边是塔里木盆地的塔克拉玛干沙漠,西南与柴达木盆地毗邻,北部是大面积的戈壁沙漠[55],因此,陆源性输入也是冰尘中DOM的重要来源,主要体现在新鲜冰尘中含有大量的低氧碳比的不饱和烃类(31.83%)和高氧碳比的不饱和烃类(18.12%),包括木质素以及单宁类化合物[56]通过风媒或干湿沉降传输到冰川表面. ...
Use of ESI-FTICR-MS to characterize dissolved organic matter in headwater streams draining forest-dominated and pasture-dominated watersheds
1
2015
... 有研究表明,冰尘是冰川表面微生物重要的聚集区[9-11],冰尘中微生物群落非常丰富[11].结合老虎沟12号冰川新鲜冰尘中DOM脂类(25.88%)和多肽类(20.11%)的含量,以及新鲜冰尘DOM的光谱斜率的比值SR=1.93(SR>1),说明新鲜冰尘中DOM主要源自冰尘内部的微生物活动[41,54].同时,老虎沟12号冰川地处干旱和半干旱环绕区,西边是塔里木盆地的塔克拉玛干沙漠,西南与柴达木盆地毗邻,北部是大面积的戈壁沙漠[55],因此,陆源性输入也是冰尘中DOM的重要来源,主要体现在新鲜冰尘中含有大量的低氧碳比的不饱和烃类(31.83%)和高氧碳比的不饱和烃类(18.12%),包括木质素以及单宁类化合物[56]通过风媒或干湿沉降传输到冰川表面. ...
Degradation of terrestrially derived macromolecules in the Amazon River
1
2013
... DOM的化学组成在整个培养过程中发生了明显的变化[表3,图4(a)].从D0至D6,多肽类化合物的相对含量从20.11%降低到17.09%,高氧碳比的不饱和烃类化合物相对含量从18.12%降低至10.96%,芳烃类化合物的相对含量从3.34%降低至3.06%,多环芳烃类化合物相对含量从0.59%降低至0.16%;其他类型的化合物相对含量都有所增加,脂类化合物的相对含量从25.88%增加至33.91%,低氧碳比的不饱和烃类化合物的相对含量从31.83%增加到34.62%,糖类从0.13%增加到0.19%.以上变化趋势说明在培养初期,生物可利用性高的多肽类分子可以快速被微生物消耗利用,同时光化学过程导致光敏感性强的芳烃类和多环芳烃类化合物相对含量均降低.从D6至D18,脂类和多肽类化合物的相对含量持续降低,脂类化合物的相对含量从33.91%降低至21%,多肽类化合物的相对含量从17.09%降低至12.76%;其他各类化合物的相对含量均表现为升高的趋势,低氧碳比的不饱和烃类化合物的相对含量从34.62%增加到37.69%,高氧碳比的不饱和烃类化合物的相对含量从10.96%增加到20.89%,芳烃类化合物的相对含量从3.06%增加到5.62%,多环芳烃类化合物的相对含量从0.16%增加到1.60%,糖类化合物的相对含量从0.19%增加到0.45%.有研究表明,具有低AImod(AImod<0.5)的不饱和烃类分子可能含有富含羧基的脂环分子[57],这类分子是一类潜在的难降解化合物,可以通过细菌代谢产生[58].Samui等[59]研究发现,南极冰盖表面冰尘穴中的微生物在光照条件下可以降低甲酸和乙酸的含量,增加乙二酸的含量.结合本研究中DOM分子组成的变化趋势,说明随着培养时间的增加,在光氧化作用和微生物的作用下,随着生物可利用性强的多肽类和脂类分子含量的明显减少,生物活性较低的不饱和烃类、芳烃类化合物和多环芳烃类化合物开始富集,其中高氧碳比的不饱和烃类含量增加最为明显,表明“光-生物”演化过程可以增加DOM分子的氧化程度和不饱和性.培养过程中冰尘水样中DOM的AImod从0.15(D0)显著升高至0.20(D18)(P<0.05)(表2)很好的印证了这一结论. ...
Marine sequestration of carbon in bacterial metabolites
1
2015
... DOM的化学组成在整个培养过程中发生了明显的变化[表3,图4(a)].从D0至D6,多肽类化合物的相对含量从20.11%降低到17.09%,高氧碳比的不饱和烃类化合物相对含量从18.12%降低至10.96%,芳烃类化合物的相对含量从3.34%降低至3.06%,多环芳烃类化合物相对含量从0.59%降低至0.16%;其他类型的化合物相对含量都有所增加,脂类化合物的相对含量从25.88%增加至33.91%,低氧碳比的不饱和烃类化合物的相对含量从31.83%增加到34.62%,糖类从0.13%增加到0.19%.以上变化趋势说明在培养初期,生物可利用性高的多肽类分子可以快速被微生物消耗利用,同时光化学过程导致光敏感性强的芳烃类和多环芳烃类化合物相对含量均降低.从D6至D18,脂类和多肽类化合物的相对含量持续降低,脂类化合物的相对含量从33.91%降低至21%,多肽类化合物的相对含量从17.09%降低至12.76%;其他各类化合物的相对含量均表现为升高的趋势,低氧碳比的不饱和烃类化合物的相对含量从34.62%增加到37.69%,高氧碳比的不饱和烃类化合物的相对含量从10.96%增加到20.89%,芳烃类化合物的相对含量从3.06%增加到5.62%,多环芳烃类化合物的相对含量从0.16%增加到1.60%,糖类化合物的相对含量从0.19%增加到0.45%.有研究表明,具有低AImod(AImod<0.5)的不饱和烃类分子可能含有富含羧基的脂环分子[57],这类分子是一类潜在的难降解化合物,可以通过细菌代谢产生[58].Samui等[59]研究发现,南极冰盖表面冰尘穴中的微生物在光照条件下可以降低甲酸和乙酸的含量,增加乙二酸的含量.结合本研究中DOM分子组成的变化趋势,说明随着培养时间的增加,在光氧化作用和微生物的作用下,随着生物可利用性强的多肽类和脂类分子含量的明显减少,生物活性较低的不饱和烃类、芳烃类化合物和多环芳烃类化合物开始富集,其中高氧碳比的不饱和烃类含量增加最为明显,表明“光-生物”演化过程可以增加DOM分子的氧化程度和不饱和性.培养过程中冰尘水样中DOM的AImod从0.15(D0)显著升高至0.20(D18)(P<0.05)(表2)很好的印证了这一结论. ...
Fate of dissolved organic carbon in Antarctic Surface Environments during Summer
1
2020
... DOM的化学组成在整个培养过程中发生了明显的变化[表3,图4(a)].从D0至D6,多肽类化合物的相对含量从20.11%降低到17.09%,高氧碳比的不饱和烃类化合物相对含量从18.12%降低至10.96%,芳烃类化合物的相对含量从3.34%降低至3.06%,多环芳烃类化合物相对含量从0.59%降低至0.16%;其他类型的化合物相对含量都有所增加,脂类化合物的相对含量从25.88%增加至33.91%,低氧碳比的不饱和烃类化合物的相对含量从31.83%增加到34.62%,糖类从0.13%增加到0.19%.以上变化趋势说明在培养初期,生物可利用性高的多肽类分子可以快速被微生物消耗利用,同时光化学过程导致光敏感性强的芳烃类和多环芳烃类化合物相对含量均降低.从D6至D18,脂类和多肽类化合物的相对含量持续降低,脂类化合物的相对含量从33.91%降低至21%,多肽类化合物的相对含量从17.09%降低至12.76%;其他各类化合物的相对含量均表现为升高的趋势,低氧碳比的不饱和烃类化合物的相对含量从34.62%增加到37.69%,高氧碳比的不饱和烃类化合物的相对含量从10.96%增加到20.89%,芳烃类化合物的相对含量从3.06%增加到5.62%,多环芳烃类化合物的相对含量从0.16%增加到1.60%,糖类化合物的相对含量从0.19%增加到0.45%.有研究表明,具有低AImod(AImod<0.5)的不饱和烃类分子可能含有富含羧基的脂环分子[57],这类分子是一类潜在的难降解化合物,可以通过细菌代谢产生[58].Samui等[59]研究发现,南极冰盖表面冰尘穴中的微生物在光照条件下可以降低甲酸和乙酸的含量,增加乙二酸的含量.结合本研究中DOM分子组成的变化趋势,说明随着培养时间的增加,在光氧化作用和微生物的作用下,随着生物可利用性强的多肽类和脂类分子含量的明显减少,生物活性较低的不饱和烃类、芳烃类化合物和多环芳烃类化合物开始富集,其中高氧碳比的不饱和烃类含量增加最为明显,表明“光-生物”演化过程可以增加DOM分子的氧化程度和不饱和性.培养过程中冰尘水样中DOM的AImod从0.15(D0)显著升高至0.20(D18)(P<0.05)(表2)很好的印证了这一结论. ...


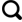



 甘公网安备 62010202000676号
甘公网安备 62010202000676号